光谱仪厂家为您解析在使用X荧光光谱仪分析时的几大误区。
1、 荧光光谱的基本原理
(1)分子荧光光谱的产生
a、分子的能级包括:电子能级(10ev)、振动能级(0.1ev)及转动能级(0.001ev)。
b、电子能级的多样性
单重态(singlet state):总自旋S=0,两个电子自旋相反,M=2S+1=1
三重态(triplet state):总自旋S=1,两个电子自旋方向平行,M=2S+1=3

2、 荧光定量分析方法
由于能产生荧光的物质占被分析物的数量相当有限,且就这少量的荧光物质几乎在同一波长段产生光致发光,所以荧光法很少用来定性分析。
(1)标准曲线法
用已知量的标准物质经过和试样相同的处理之后,配成一系列标准溶液,测定这些溶液的荧光强度,以荧光强度为纵坐标,标准溶液的浓度为横坐标绘制标准曲线。然后在同样条件下测定试样溶液的荧光强度,从标准曲线上求出试样中荧光物质的含量。
(2)比例法
取已知量的纯净荧光物质配一标液,使浓度在线性范围内,测Fs。同样条件下测试样Fx(若空白液的荧光强度调不到0%时,应扣除空白F0)。
3、 分子荧光光谱法的特点
(1)灵敏度高
(2)选择性强
(3)样品用量少
(4)信息量丰富
(5)方便、快捷
(6)环保
4. 跃迁类型的比较
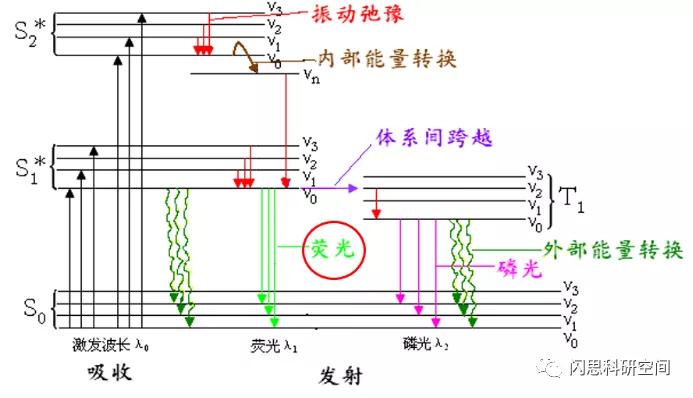
处于激发态的分子返回到基态共有以下几种途径:
a、振动驰豫(vibrationalrelexation):
特点:发生在同一个激发态的电子能级上;时间约10-12秒。
b、内部能量转换(internal conversion):
特点:两个电子的能级非常靠近以致其振动能级有重叠时内部转换易发生。10-1~10-13秒可完成。
c、外部能量转换(external conversion):
特点:发生分子与分子的碰撞时;时间约10-9~10-7秒。
d、体系间跨越(intersystem crossing):
特点:振动能级重迭时,产生体系间跨越的可能大;跨越后,荧光量子减弱,甚至会荧光熄灭。
e、荧光(Fluorescence):
特点:荧光的能量小于所吸收的紫外光的能量,故发射荧光的波长比吸收的紫外光波长更长;时间约为10-9~10-7。
f、磷光(Phosphorescence):
特点:磷光能量比荧光小,波长比荧光长;发射时间长,约为10-4~10秒(原因是分子激发三重态的寿命较长)。
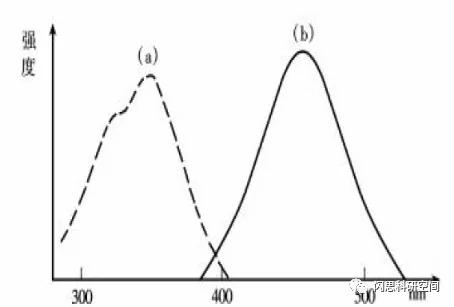
X荧光光谱仪分析曲线
5. 荧光光谱的特点
a、斯托克斯位移(Stocks shift):荧光发射波长总是大于激发光波长。原因:激发态分子由于内部能量转换和振动驰豫过程而迅速到达S1*电子态的最低振动能级,从而存在着无辐射能量损失。
b、荧光发射光谱的形状与激发波长无关。原因:荧光发射发生于第一电子激发态的最低能级,与分子激发至那一个电子能级无关(即使分子激发到高于S1*的电子态的更高振动能级,可通过内转换和振动驰豫等无辐射跃迁的形式释放能量回到第一电子激发态的最低能级)。
c、荧光光谱与激发光谱呈对称镜像关系。
6、 分子荧光光谱的主要应用
(1)在生物领域的应用该领域主要用于临床测定生物样品中某些成分的含量,生物技术及免疫技术的分析等,如脱氧核糖和脱氧核糖核酸的含量测定、DNA、抗体、抗原等各方面的研究。在此领域中主要时利用各种荧光探针进行分析检测,主要分为生物纳米荧光探针和生物非纳米荧光探针。
(2)在食品领域的应用该领域主要用于食品中矿物质及金属元素、氨基酸、维生素、菌类污染、添加剂、防腐剂、食品包装有害物质、农药残留等的分析检测。特别是与HPLC、TLC、FIA等技术的结合可以更好的达到食品中各种物质的检测效果。
(3)分子荧光光谱在药物分析中的应用药物分析领域可以利用荧光分析进行药物的有效成分鉴定、药物代谢动力学研究、临床药理药效分析等。药物荧光分析可以分为三类:直接荧光分析、间接荧光分析和纳米荧光分析。
(4)分子荧光光谱在环境分析中的应用该领域主要利用荧光分析检测环境中的物质的含量,主要是对水体、矿石和土壤进行检测。
